La crainte est que la manipulation génétique puisse également être appliquée pour essayer d'améliorer les performances sportives ; en ce sens, l'Agence mondiale antidopage (AMA) a déjà pris des mesures, en incluant le dopage génétique dans la liste des méthodes et substances interdites.
En théorie, tous les niveaux de protéines présentes dans notre corps peuvent être modulés par la thérapie génique.
La conférence sur le dopage génétique qui s'est tenue en mars 2002 par l'AMA [Pound R, WADA 2002], et le "Congrès européen du travail sur l'harmonisation et les développements futurs de la politique antidopage" qui s'est tenu à Arnhem, aux Pays-Bas, dans le même année, a donné la possibilité aux scientifiques, médecins, médecins, gouvernements, organisations antidopage et industries pharmaceutiques, d'échanger tout type d'informations sur les résultats des recherches et les méthodes de détection concernant cette nouvelle technique de dopage. .
Depuis le 1er janvier 2003, le Comité International Olympique (CIO) a inscrit le dopage génétique dans la liste des classes et méthodes de substances interdites [AMA, 2007]. Depuis 2004, l'AMA a pris la responsabilité de publier la liste internationale du dopage, qui est mise à jour chaque année. La méthode de dopage génétique incluse dans cette liste est définie comme l'utilisation non thérapeutique de cellules, de gènes, d'éléments génétiques ou la modulation de l'expression des gènes, dans le but d'améliorer les performances sportives.
Cet article vise à :
- de préciser si, dans le sport, il est effectivement possible d'exploiter les connaissances croissantes issues de la thérapie génique, une branche nouvelle et prometteuse de la médecine traditionnelle ;
- identifier les voies possibles d'utilisation de la thérapie génique pour augmenter les performances.
En cette « ère de la génétique et de la génomique, il sera possible d'identifier les gènes qui déterminent la prédisposition génétique d'une personne pour un sport spécifique [Rankinen T et al., 2004]. L'étude des gènes à un jeune âge peut représenter le meilleur moyen de développer un grand athlète à partir d'un enfant et de créer un programme d'entraînement personnel spécifique. Cette étude appliquée aux athlètes peut également être utilisée pour identifier des méthodes d'entraînement spécifiques dans le but d'augmenter la prédisposition génétique pour ce type d'entraînement [Rankinen T et al., 2004].
Mais l'étude des gènes aboutira-t-elle à de meilleurs athlètes ?
Marion Jones et Tim Montgomery étaient tous les deux champions de vitesse du 100 m, ils ont eu un bébé à l'été 2003. Steffi Graf et Andre Agassi (tous deux champions du monde de tennis) ont aussi des enfants. Ces enfants seront très probablement les favoris par rapport aux autres, mais il y a aussi d'autres facteurs, tels que les facteurs environnementaux et psychologiques, qui détermineront ou non la possibilité qu'ils deviennent des champions.
La thérapie génique peut être définie comme le transfert de matériel génétique dans des cellules humaines pour le traitement ou la prévention d'une maladie ou d'un dysfonctionnement. Ce matériel est représenté par l'ADN, l'ARN ou par des cellules génétiquement modifiées. Le principe de la thérapie génique repose sur l'introduction dans la cellule d'un gène thérapeutique pour compenser le gène manquant ou remplacer celui anormal. Généralement, on utilise de l'ADN qui code pour la protéine thérapeutique et est activé lorsqu'il atteint le noyau.
"La plupart des athlètes se dopent" [De Francesco L, 2004].
Une enquête du Drug Research Center a conclu que moins de 1% de la population néerlandaise a pris des produits dopants au moins une fois, pour un total d'environ 100 000 personnes. 40 % de ces personnes ont recours au dopage depuis des années et la plupart font de la musculation ou de la musculation. L'usage de substances dopantes dans le sport d'élite semble être supérieur aux 1% indiqués pour la population générale, mais le chiffre exact n'est pas connu.Le pourcentage d'athlètes d'élite testés positifs aux contrôles antidopage a fluctué entre 1%. 2,0 % ces dernières années [DoCoNed, 2002].
La définition de l'AMA du dopage génétique laisse place à des questions
- Que signifie exactement non thérapeutique ?
- Les patients atteints de dysfonctions musculaires traités par thérapie génique seront-ils admis aux compétitions ?
La même considération s'applique aux patients cancéreux qui ont été traités par chimiothérapie et qui reçoivent maintenant le gène EPO codant pour l'érythropoïétine pour accélérer la récupération de la fonction de la moelle osseuse.
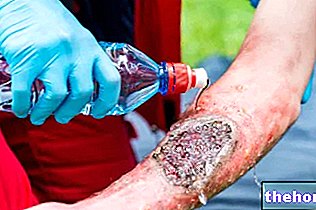
Les recherches actuelles en thérapie génique sont également menées pour accélérer le processus de cicatrisation d'une plaie ou pour soulager les douleurs musculaires après l'exercice ; de telles pratiques peuvent ne pas être considérées par tous comme « thérapeutiques » et leurs propriétés d'amélioration des performances peuvent être remises en question.
D'un point de vue clinique, il serait plus approprié de mieux préciser la définition du dopage génétique, notamment à la lumière d'une mauvaise utilisation des technologies de transfert de gènes.
AMA (section M3 de la Code mondial antidopage (version 1er janvier 2007) a justifié l'interdiction du dopage génétique par les points suivants :
- preuve scientifique, effet pharmacologique prouvé ou expérience, que les substances ou méthodes incluses dans la liste ont la capacité d'augmenter les performances sportives ;
- l'utilisation de la substance ou de la méthode entraîne un risque réel ou présumé pour la santé du sportif.
- l'usage du dopage viole l'esprit du sport.Cet esprit est décrit dans l'introduction du Code en référence à une série de valeurs telles que l'éthique, le fair-play, l'honnêteté, la santé, le plaisir, le bonheur et le respect des règles.
Il existe de nombreuses incertitudes concernant les effets à long terme de la modification génétique ; bon nombre de ces effets peuvent également ne jamais être découverts, soit parce qu'ils n'ont pas été étudiés à fond (en raison de problèmes financiers), soit parce qu'il est difficile de définir des échantillons fiables pour étudier les effets secondaires de méthodes ou d'applications complètement nouvelles.
Contrairement aux thérapies cellulaires somatiques, les altérations des lignées germinales sont permanentes et se transmettent également à la descendance. Dans ce cas, outre le risque éventuel pour la santé des sportifs, il existe également des risques vis-à-vis des tiers, tels que la postérité, les parents ou les partenaires.
Dans le domaine de la pharmacogénétique, dont le développement dépend des efforts conjugués de la science et de l'industrie pharmaceutique, l'objectif principal est de développer une médecine « sur mesure » pour chacun d'entre nous. sur qui les prend, cela est dû au fait que leur développement est générique et ne prend pas en compte les caractéristiques génétiques individuelles. Si la pharmacogénétique devait se répandre dans le monde du sport, l'idée même de compétition entre athlètes apparemment égaux qui se préparent de manière plus ou moins comparable pourrait devenir obsolète.
Les données cliniques expérimentales de thérapie génique ont montré des résultats très encourageants chez des patients présentant un déficit immunitaire combiné sévère [Hacein-Bey-Abina S et al., 2002] et une hémophilie B [Kay MA, et al. 2000]. De plus, la thérapie angiogénique par des vecteurs exprimant le facteur de croissance endothélial vasculaire pour le traitement des maladies coronariennes a donné de bons résultats dans l'angine [Losordo DW et al., 2002].
Si le transfert de gènes codant pour les facteurs de croissance tissulaire était utilisé [Huard J, Li Y, Peng HR, Fu FH, 2003], le traitement des divers dommages liés à la pratique sportive, tels que la rupture ligamentaire, ou la déchirure musculaire, pourrait théoriquement en résulter. dans une meilleure régénération. Ces approches sont actuellement en cours d'évaluation sur des modèles animaux, mais des essais cliniques sur l'homme seront certainement également activés dans les années à venir.
En 1964, le skieur finlandais du Nord Eero Mäntyranta a rendu inutiles les efforts de ses adversaires en remportant deux médailles d'or olympiques aux Jeux d'Innsbruck, en Autriche. Après quelques années, il a été démontré que Mantyranta portait une mutation rare dans le gène du récepteur de l'érythropoïétine qui, en compromettant le rétrocontrôle normal du nombre de globules rouges, provoque une polyglobulie avec une augmentation conséquente de 25 à 50 % du capacité de transport d'oxygène. Augmenter la quantité d'oxygène dans les tissus signifie augmenter la résistance à la fatigue. Mäntyranta avait ce que chaque athlète veut : l'EPO. Les athlètes du futur pourraient être en mesure d'introduire un gène dans le corps qui imite l'effet de la mutation génétique qui s'est produite naturellement dans Mäntyranta et propice à la performance.
Le facteur de croissance analogue à l'insuline (IGF-1) est produit à la fois par le foie et le muscle et sa concentration dépend de celle de l'hormone de croissance humaine (hGH).
L'entraînement, suggère Sweeney, stimule les cellules précurseurs musculaires, appelées « satellites », pour qu'elles soient plus « réceptives à l'IGF-I.
[Lee S. Barton ER, Sweeney HL, Farrar RP, 2004]. Appliquer ce traitement aux sportifs reviendrait à renforcer les muscles brachiaux du joueur de tennis, le mollet du coureur ou les biceps du boxeur. Une telle thérapie est considérée comme relativement plus sûre que l'EPO, puisque l'effet est localisé uniquement au muscle cible. Il est probable que cette approche sera également appliquée aux personnes dès les prochaines années.
Une isoforme du facteur de croissance analogue à l'insuline-1 (IGF-1), le facteur de croissance mécanique (MGF), est activée par des stimuli mécaniques, tels que par ex. exercice musculaire.Cette protéine, en plus de stimuler la croissance musculaire, joue un rôle important dans la réparation des tissus musculaires lésés (comme cela arrive par exemple après un entraînement intensif ou une compétition).
Le MGF est produit dans le tissu musculaire et ne circule pas dans le sang.
Le VEGF représente le facteur de croissance de l'endothélium vasculaire et peut être utilisé pour faciliter la croissance de nouveaux vaisseaux sanguins.La thérapie VEGF a été développée pour produire un pontage aorto-coronarien chez les patients atteints de cardiopathie ischémique, ou pour aider les personnes âgées atteintes de maladie artérielle périphérique. ce code pour le VEGF peut favoriser la croissance de nouveaux vaisseaux sanguins en permettant un plus grand apport d'oxygène aux tissus.
Jusqu'à présent, des expériences de thérapie génique ont été menées pour des maladies telles que l'ischémie cardiaque [Barton-Davis ER et al., 1998; Losordo DW et al., 2002; Tio RA et al., 2005], ou l'insuffisance artérielle périphérique [Baumgartner I et al., 1998; Rajagopalan S et al., 2003].
Si ces traitements étaient également appliqués aux sportifs, il en résulterait une augmentation de la teneur en oxygène et en nutriments des tissus, mais surtout la possibilité de retarder l'épuisement du muscle cardiaque et du muscle squelettique.
Le VEGF étant déjà utilisé dans de nombreux essais cliniques, le dopage génétique serait déjà possible.
Le normal différenciation de la masse musculo-squelettique elle est d'une importance fondamentale pour le bon fonctionnement de l'organisme ; cette fonction est rendue possible grâce à l'action de la myostatine, une protéine responsable de la croissance et de la différenciation des muscles squelettiques.
Il agit comme un régulateur négatif, inhibant la prolifération des cellules satellites dans les fibres musculaires.
Expérimentalement, la myostatine est utilisée in vivo pour inhiber le développement musculaire dans différents modèles de mammifères.
La myostatine est active à la fois avec un mécanisme autocrine et paracrine, à la fois au niveau musculo-squelettique et cardiaque.Son rôle physiologique n'est pas encore entièrement compris, bien que l'utilisation d'inhibiteurs de la myostatine, tels que la follistatine, provoque une augmentation spectaculaire et généralisée de la masse musculaire [Lee SJ, McPherron AC, 2001]. De tels inhibiteurs peuvent améliorer l'état de régénération chez les patients souffrant de maladies graves telles que la dystrophie musculaire de Duchenne [Bogdanovich S et al., 2002)].
La myostatine appartient à la superfamille des TGF bêta et a été révélée pour la première fois par le groupe de Se-Jin Lee [McPherron et al., 1997]. En 2005, Se-Jin Lee de l'Université Johns Hopkins a souligné que les souris privées du gène de la myostatine (souris knock-out) développent une musculature hypertrophique.
Ces supersouris étaient capables de monter des escaliers avec des poids lourds attachés à leur queue. Au cours de la même année, trois autres groupes de recherche ont montré que le phénotype bovin communément appelé « double-muscle » était dû à une mutation du gène codant pour la myostatine [Grobet et al., 1997 ; Kambadur et al., 1997 ; McPherron et Lee, 1997].
Une mutation du type homozygote mstn - / - a été récemment découverte chez un enfant allemand qui a développé une masse musculaire extraordinaire. La mutation a été désignée comme l'effet d'inhibition de l'expression de la myostatine chez l'homme. L'enfant a bien développé ses muscles à la naissance, mais en grandissant a également augmenté le développement de la masse musculaire et à l'âge de 4 ans, il était déjà capable de soulever des poids de 3 kilos ; il est le fils d'un ancien athlète professionnel et ses grands-parents étaient connus comme des hommes très forts.
Les analyses génétiques de la mère et de l'enfant ont révélé une mutation du gène de la myostatine entraînant un manque de production de la protéine [Shuelke M et al., 2004].
Tant dans le cas des expériences menées sur la souris par le groupe Se-Jin Lee que dans celui de l'enfant, le muscle s'était développé à la fois en section transversale (hypertrophie) et en nombre de myofibrilles (hyperplasie) [McPherron et al. ., 1997].
La douleur est une expérience sensorielle et émotionnelle désagréable associée à des lésions tissulaires réelles ou potentielles et décrite en termes de telles lésions [iasp]. De par son caractère désagréable, l'émotion de la douleur ne peut être ignorée et induit le sujet qui l'essaie à éviter les stimuli (nocifs) qui en sont responsables ; cet aspect configure la fonction protectrice de la douleur.
Dans le sport, l'utilisation de puissants analgésiques pourrait amener les athlètes à s'entraîner et à concourir au-delà du seuil de douleur normal.
Cela peut entraîner des risques considérables pour la santé de l'athlète, car la blessure peut s'aggraver considérablement, se transformer en blessure permanente.L'utilisation de ces drogues peut également conduire l'athlète à une dépendance psycho-physique à leur égard.
Une "alternative aux analgésiques légaux pourrait être d'utiliser des peptides analgésiques tels que les endorphines ou les enképhalines. La recherche animale préclinique a montré que les gènes codant ces peptides ont un effet sur la perception de la douleur inflammatoire [Lin CR et al. , 1999].
Cependant, la thérapie génique pour le soulagement de la douleur est encore loin de son application clinique.
, produits chimiques, virus, etc.) et le transgène codé.La recherche clinique à ce jour a été relativement sûre [Kimmelman J, 2005]. Plus de 3000 patients ont été traités et un seul d'entre eux est décédé d'une maladie hépatique chronique et d'une overdose de vecteurs [Raper SE et al., 2003]. Chez trois autres patients traités pour un syndrome d'immunodéficience, des symptômes de type leucémie se sont développés [Hacein-Bey-Abina S et al., 2002] et l'un d'eux est décédé. Depuis lors, d'autres groupes de recherche ont traité des patients similaires avec des résultats thérapeutiques similaires, sans aucun effet secondaire [Cavazzana-Calvo M. Fischer A, 2004]. Dans ce cas, la recherche vise à traiter les patients avec des vecteurs qui ne peuvent jamais être utilisés pour améliorer les performances.
Les personnes qui essaient d'augmenter leurs niveaux d'EPO de manière anormale augmentent également la probabilité de subir des crises cardiaques ou des épisodes cérébraux aigus. L'augmentation du nombre de globules rouges détermine également une augmentation de la densité sanguine qui peut provoquer des caillots sanguins, il n'est donc pas faux de penser que les effets indésirables observés chez les patients peuvent également survenir chez les sportifs sains [Lage JM et al., 2002].
Si l'EPO était introduite génétiquement, le niveau et la durée de la production d'érythropoïétine seraient moins contrôlables, de sorte que l'hématocrite progresserait presque indéfiniment jusqu'à des niveaux pathologiques.
Il est supposé que le traitement avec IGF-1 peut conduire à la croissance de tumeurs hormono-dépendantes.
Il est donc d'une importance cruciale que l'utilisation de vecteurs sélectionnés de manière pharmacogénétique ait un modèle d'expression génique bien connu et contrôlé.
Les méthodes exactes de détection du dopage génétique n'ont pas encore été établies, également parce que l'ADN qui est transféré avec la thérapie génique est d'origine humaine, donc pas différent de celui des athlètes qui l'utilisent.
Les thérapies musculaires sont confinées au site d'injection ou aux tissus à proximité immédiate, par conséquent, la plupart des technologies géniques sur les muscles ne pourront pas être détectées par l'analyse antidopage classique des échantillons d'urine ou de sang ; une biopsie musculaire serait nécessaire, mais elle est trop invasive pour être conçue comme un moyen normal de contrôle antidopage.
De nombreuses formes de dopage génétique ne nécessitent pas l'introduction directe de gènes dans l'organe souhaité ; le gène de l'EPO, par exemple, peut être injecté dans n'importe quelle partie du corps et produire localement la protéine qui entrera ensuite dans la circulation.Rechercher le site d'injection de l'EPO serait comme chercher une aiguille dans une botte de foin.
Dans la plupart des cas, cependant, le dopage génétique se traduira par l'introduction d'un gène qui est une copie exacte de l'endogène et capable de donner naissance à une protéine totalement identique à l'endogène dans ses modifications post-traductionnelles.
Une publication récente indique qu'il est possible de détecter une différence entre la protéine innée et le produit de thérapie génique basée sur les différents schémas de glycosylation dans différents types cellulaires, il reste à voir si c'est le cas avec tous les types de dopage génétique. Lasne F et al., 2004].
Les pouvoirs publics et les organisations sportives, dont le Comité International Olympique, ont condamné le dopage dès les années 1960. Les avancées récentes des produits biologiques auront un impact majeur sur la nature des médicaments prescrits aux patients, et modifieront également le choix des médicaments utilisés pour améliorer les performances sportives.
La thérapie génique est autorisée exclusivement pour les essais cliniques de produits de thérapie génique somatique chez l'homme, excluant strictement la possibilité de considérer tout type de thérapie génique germinale humaine comme faisable.
L'interdiction du dopage génétique par l'Agence mondiale antidopage (AMA) et les fédérations sportives internationales constitue une base solide pour son élimination dans le sport, mais dépendra aussi de la manière dont les différents règlements seront reçus par les athlètes.
La plupart des athlètes n'ont pas suffisamment de connaissances pour comprendre pleinement l'effet négatif potentiel du dopage génétique. Pour cette raison, il sera très important qu'eux-mêmes et leur personnel d'encadrement soient bien formés, afin d'éviter son utilisation. Les athlètes doivent également être conscients des risques associés à l'utilisation du dopage génétique lorsqu'il est utilisé dans des installations non contrôlées, sans toutefois compromettre le potentiel infini offert par la thérapie génique officielle pour le traitement des pathologies graves.
L'industrie pharmaceutique est bien consciente des possibilités et des risques liés à l'utilisation du dopage génétique et souhaite collaborer au développement de la recherche pour la détection des produits géniques présents dans ses médicaments. Il devra de préférence signer un code dans lequel il s'engage à ne jamais produire ni vendre, pour quelque raison que ce soit, des produits génétiques à usage non thérapeutique.
Un nombre limité de personnes issues de différentes disciplines de la science et du sport ont été interrogées, afin de se faire « une idée de la notion et de l'impact possible du dopage génétique sur elles. Parmi les personnes interrogées il y avait trois médecins du sport, un pharmacien, quatre athlètes d'élite et cinq scientifiques du monde universitaire et de l'industrie pharmaceutique ; voici les questions :
- Connaissez-vous le terme dopage génétique ?
- A votre avis, que signifie ce terme ?
- Croyez-vous à l'amélioration des performances grâce à l'utilisation du dopage génétique ?
- Quels sont, selon vous, les risques pour la santé liés au recours au dopage génétique ?
- Le dopage génétique est-il déjà utilisé ou ne le sera-t-il que dans le futur ?
- Sera-t-il facile de détecter le dopage génétique ?
D'après les différentes réponses, il est clair que les personnes extérieures à la communauté scientifique ont peu de connaissances sur l'utilisation de cette thérapie ; une crainte commune est que la thérapie génique puisse affecter la progéniture, ou provoquer un cancer. Le dopage génétique sera complexe et les mesures préventives difficiles. d'autre part, tout le monde insiste sur le fait que le dopage génétique sera utilisé par les athlètes dès qu'il sera disponible et que cela se produira dans les prochaines années.
Les professionnels qui entourent les sportifs d'élite sont très préoccupés par l'utilisation possible du dopage génétique et recommandent l'éducation de leurs sportifs et de leur personnel d'encadrement médical, en soutien au développement de la recherche préventive sur la mesure antidopage.Ces professionnels sont convaincus que le problème de l'application du dopage génétique aux athlètes se posera au cours des prochaines années et que sa détection sera plutôt difficile.
Le monde du sport se trouvera tôt ou tard confronté au phénomène du dopage génétique ; le nombre exact d'années qui devront s'écouler pour que cela se produise est difficile à estimer, mais on peut supposer que cela se produira bientôt, dans les prochaines années (Jeux olympiques de Pékin 2008 ou au plus tard les suivants).
Du cyclisme à l'haltérophilie, de la natation au soccer et au ski, tous les sports pourraient bénéficier de la manipulation génétique : il suffit de sélectionner le gène qui améliore le type de performance requis ! [Bernardini B., 2006].