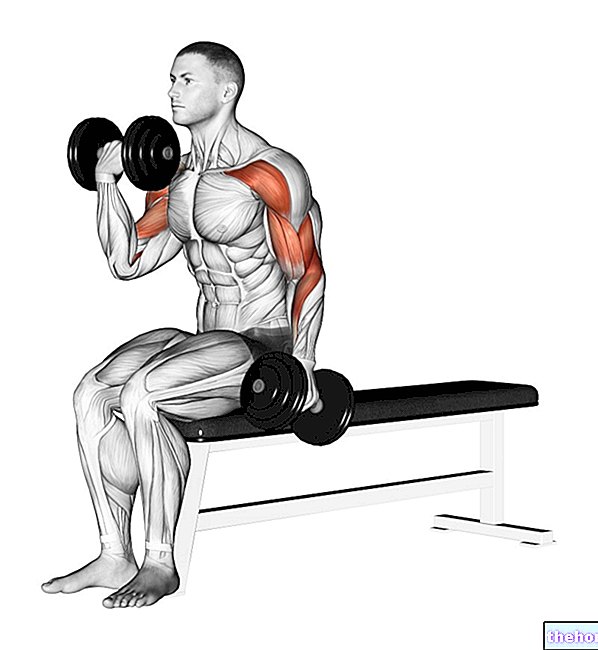
L'activité la plus connue de la carnitine est son rôle de transporteur d'acides gras à longue chaîne dans la matrice mitochondriale, où les acides gras sont convertis en énergie grâce au processus de bêta-oxydation. et terrains de sport.
de sa carnitine totale, qui correspond au total à 25 %.La synthèse endogène s'effectue à partir du substrat TML (6-N-triméthylsine), qui à son tour dérive de la méthylation de l'acide aminé lysine.La TML est ensuite hydroxylée en hydroxyméthyline (HTML) au moyen de la trimoxylismine dioxygénase, ce qui nécessite la présence d'acide ascorbique et de fer. Le HTML est ensuite décomposé par l'HTML aldolase (un phosphate de pyridoxal qui nécessite l'enzyme), produisant du 4-triméthylaminobutyraldéhyde (TMABA) et de la glycine. Le TMABA est ensuite déshydrogéné en gamma-butyrobétaïne dans une réaction dépendante du NAD+, catalysée par la TMABA déshydrogénase. La gamma-butyrobétaïne est ensuite hydroxylée par la gamma-butyrobétaïne hydroxylase (une enzyme de liaison de) en L-carnitine, qui nécessite du fer sous forme de Fe2+.
En résumé:
- La 6-N-triméthyllysine (TML) est obtenue par méthylation de la lysine
- Grâce à la trimoxylsyoxygénase, en présence de fer et d'acide ascorbique (vitamine C), la TML est hydroxylée en hydroxyméthylline (HTML)
- Par aldolase, le HTML est décomposé en 4-triméthylaminobutyraldéhyde (TMABA) + glycine
- Grâce à l'action de la TMABA déshydrogénase et à la catalyse du NAD+, le TMABA est déshydrogéné en gamma-butyrobétaïne
- Grâce à l'activité de la gamma butyrobétaïne hydroxylase, la gamma-butyrobétaïne est ensuite hydroxylée en L-carnitine, qui nécessite du fer sous forme de Fe2+.