1) PROTÉINES CIBLES
Voici quelques exemples de cibles protéiques. Dans le premier exemple, nous considérons une « hémoprotéine qui est l'hémoglobine », et un toxique très similaire, qui est le monoxyde de carbone (CO). Le monoxyde de carbone, 250 fois plus similaire que l'oxygène, se lie au groupe -EME de l'hémoglobine, empêchant ainsi le transport de l'oxygène.Les cellules tissulaires meurent d'HYPOXIE ANÉMIQUE car elles ne reçoivent pas l'oxygène nécessaire à la respiration cellulaire.
Dans le deuxième exemple, une molécule de protéine enzymatique est prise en considération, qui est la Cyt C oxydase, et le toxique associé, le cyanure. La Cyt C oxydase est une enzyme qui appartient à la chaîne de transport d'électrons. La respiration cellulaire se produit au niveau de la mitochondrie et la Cyt C oxydase exploite l'oxygène pour assurer que quatre ions H + sont expulsés de la mitochondrie ; cette expulsion d'ions hydrogène forme la différence de potentiel nécessaire à la synthèse d'ATP. L'enzyme est bloquée par le cyanure , la Cyt C oxydase n'utilise plus d'oxygène moléculaire, le gradient optimal de protons ne se forme pas en dehors de la mitochondrie ; par conséquent, la cellule ne synthétise pas d'ATP. Dans ce cas également, les cellules vont à l'encontre de la mort due à l'hypoxie ; on parle notamment d'HYPOXIE CYTOTOXIQUE.
Parmi toutes les cibles protéiques, on trouve les récepteurs qui ont été expliqués en pharmacologie générale. Les toxines les plus importantes, telles que la nicotine et la strychnine, peuvent interagir avec divers récepteurs.
2) CIBLES LIPIDES
Les lipides les plus touchés par les radicaux libres sont ceux de la membrane. Le radical libre, du point de vue chimique, se forme car il n'y a pas d'"hétérolyse" entre deux atomes, donc deux ions avec une charge homogène ne se forment pas, mais il y a une "homolyse".
L'homolyse se caractérise par une répartition inégale des charges.

Les radicaux libres se forment à partir de substances externes (xénobiotiques), mais aussi à l'intérieur de notre organisme (radicaux libres d'oxygène). On peut donc dire que les radicaux libres peuvent se former aussi bien de l'extérieur que de l'intérieur de notre organisme.
Comment ces radicaux se forment-ils ?
Des radicaux libres d'oxygène peuvent se former lorsqu'il y a un changement dans la tension partielle d'oxygène dans la cellule, il y a donc des changements soudains de la pression d'oxygène. Ces manques soudains d'oxygène favorisent la formation d'espèces radicalaires dans les tissus ischémiques (cerveau) ou cardiaques. Les espèces radicalaires de l'oxygène sont principalement l'ANION SUPEROXYDE et l'OXIDRILE.Le manque d'antioxydants (vitamines A, C et E), le vieillissement cellulaire, les xénobiotiques et enfin les états inflammatoires aigus et/ou chroniques sont autant de phénomènes qu'ils peuvent conduire à la formation de radicaux libres.

La cellule peut réagir à ces dommages possibles dus à l'apparition de radicaux libres d'oxygène, car elle possède des enzymes particulières qui contrecarrent l'activité des radicaux.

3) GROUPES CIBLES - SH
La troisième cible est constituée des groupes SH des protéines, qui sont oxydés par les radicaux libres d'oxygène.
Les protéines les plus endommagées par les radicaux libres sont :
- Toutes les protéines du cytosquelette qui possèdent des groupes -SH, telles que l'actine et la tubuline ;
- Protéines intégrales de la membrane plasmique;
- Tous les systèmes membranaires de transduction du signal.
- Les protéines de la membrane mitochondriale ;
- ATPase qui transporte l'ion calcium hors de la cellule (l'accumulation de calcium dans la cellule conduit à la mort cellulaire) ;
- La protéineKinase C ;
Le glutathion (GSH) protège la cellule du stress oxydatif. Le glutathion parvient à désactiver l'action du peroxyde d'hydrogène grâce au GPO (glutathion peroxydase).
Le GSH oxydé peut être à nouveau réduit s'il a du NADPH disponible ; s'il n'y a pas de "NADPH ou c" il y a trop de peroxyde d'hydrogène, le GSH ne pourra pas revenir sous une forme réduite, il ne sera donc plus fonctionnel contre le stress oxydatif.
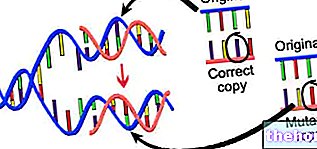
4) CIBLES D'ACIDE NUCLEIQUE
La cible des substances toxiques sont les acides nucléiques, qui sont formés par des paires de bases pyrimidine et purine. Les composés xénobiotiques qui agissent comme agents alkylants des bases puriques et pyrimidiques empêchent la synthèse et la réplication du brin d'ADN. Parmi ces substances dangereuses, nous trouvons les NITROSAMINES qui se forment entre les nitrites, utilisés comme conservateurs dans les viandes et les saucisses, et les amines aromatiques secondaires issues de différents modes de cuisson.
A l'intérieur de l'estomac, où le pH est très acide, les nitrites et les amines aromatiques secondaires réagissent, formant des nitrosamines, dont la fonction est très dangereuse pour le brin d'ADN.
L'AFLATOXINE est une autre substance toxique qui agit comme agent d'alkylation de l'ADN. Ce dernier est une mycotoxine responsable de la pollution des céréales. Une fois pénétré dans notre corps, il est métabolisé avec la formation d'un métabolite époxy responsable de l'effet alkylant.
Comme on peut le déduire, les nitrosamines se forment à l'intérieur de notre corps à partir d'une réaction entre deux composés introduits par les aliments, tandis que l'aflatoxine est introduite dans notre corps à la suite de céréales contaminées.
En plus des principaux dommages causés par une réplication incorrecte de l'ADN, il peut y avoir une formation possible de mauvais triplets de base, qui synthétisent les mauvais acides aminés. Une fragmentation de l'ADN peut également se produire, avec pour conséquence la destruction des molécules qui constituent les bases (ouverture du cycle imidazole), avec formation finale du radical hydroxyle. Avec l'ouverture du cycle imidazole, la réplication de l'ADN est bloquée. , les réticulations peut provenir entre les bases (CROSSING LINKING) d'un même brin ou de brins complémentaires En raison de la formation de ces liaisons, le brin d'ADN ne se sépare pas lors de la réplication.
En résumé, les dommages possibles à l'ADN dus à des substances toxiques sont :
- FORMATION D'ADDUCTS (alkylation de l'ADN);
- FRAGMENTATION D'ADN (ouverture du « cycle imidazole avec bloc de réplication) ;
- FORMATION DE LIAISONS CROISÉES ENTRE LES BASES (échec du filament à s'ouvrir lors de la réplication).
Avec la quatrième cible se termine la partie où les cibles possibles des toxicomanes sont expliquées.
Autres articles sur "Molécules cibles de substances toxiques"
- Toxicodynamique
- Toxicité et toxicologie
- Réactions entre cible toxique et cible biologique


















.jpg)






